
Abstrakt
For nylig er Nanjing Liming Bio-Products Co., Ltd. (www.leimingbio.com) SARS-COV-2 LGM/IgG Antistof Rapid Test Kit blevet certificeret af det brasilianske nationale sundhedsovervågningsbureau og opnået ANVISA-certificeringen. På samme tid er SARS-COV-2 RT-PCR og IgM/IgG Antistof Rapid Test Kit også anført på den officielle anbefalede indkøbsliste over Indonesien. I mellemtiden er det at opløste bio -stærkt trin®Ny Coronavirus (SARS-CoV-2) Multiplex Real-Time PCR-kit, blev godkendt af Singapore Health Sciences Authority (HSA) og opnåede HSA-certifikatet.

Billede 1 Brasilien Anvisa -certificering
Brasilien (Anvisa) certificering
Anvisa, kendt som Agência Nacional de Vigilância Sanitária, er den brasilianske regulator for medicinsk udstyr. Det er nødvendigt for en virksomhed at blive registreret hos Anvisa, National Health Supervision Agency, at sælge medicinsk udstyr lovligt i Brasilien. For at blive certificeret skal de medicinske udstyr, der kommer ind i Brasilien, opfylde kravene i den brasilianske GMP sammen med de specifikke standarder, der er fastsat af de brasilianske myndigheder. I Brasilien klassificeres IVD -medicinske udstyr i klasse I, II, III og IV i henhold til risikoniveauet fra lav til høj. For klasse I- og II -produkter vedtages Kadastro -metoden, mens til klasse III og IV -produkter anvendes Registro -metoden. Efter en vellykket registrering vil et registreringsnummer blive udstedt af Anvisa, og dataene vil blive uploadet til den brasilianske database for medicinsk udstyr, dette nummer og dets tilsvarende registreringsoplysninger vises på Dou (Diário Oficial Da União).


Billede 2 Singapore Health Sciences Authority (HSA) certifikat


Billede 3 Den officielle anbefalede indkøbsliste over Indonesien

Billede 4 StrongStep®SARS-CoV-2 IgM/IgG Antistof Rapid Test
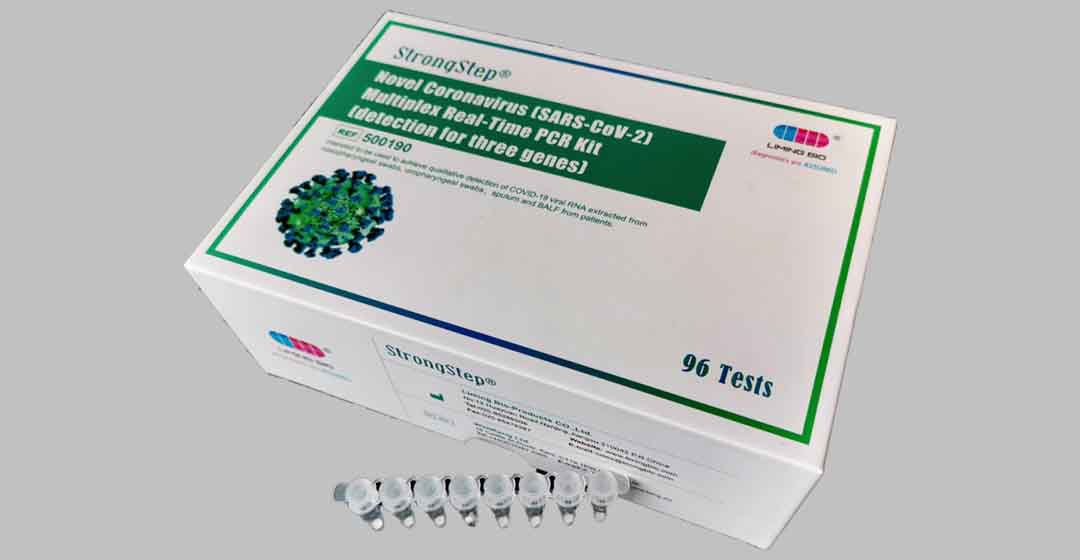
Billede 5 Novel Coronavirus (SARS-CoV-2) Multiplex Real-Time PCR Kit
Note:
Dette meget følsomme, klar til brug PCR-kit fås i lyofiliseret format (frysetørringsproces) til langtidsopbevaring. Sættet kan transporteres og opbevares ved stuetemperatur og er stabilt i et år. Hvert rør af Premix indeholder alle de reagenser, der er nødvendige til PCR-amplificering, inklusive omvendt-transkriptase, TAQ-polymerase, primere, sonder og DNTP'er. Den behøver kun tilsæt 13ul destilleret vand og 5ul ekstraheret RNA -skabelon, så kan den køres og amplificeres på PCR -instrumenterne.
Sværhedsgraden ved Cold Chain -transport af nye coronavirus -nukleinsyretektionsreagens
Når konventionelle nukleinsyretektionsreagenser transporteres i lang afstand, kræves (-20 ± 5) ℃ opbevaring og transport af koldkæde for at sikre, at bioaktivt af enzymet i reagenserne forbliver aktive. For at sikre, at temperaturen når standarden, er der behov for flere kg tøris tøris til hver kasse med nukleinsyretestreagens endnu mindre end 50 g, men den kan kun vare i to eller tre dage. På perspektivet af industriens praksis er den faktiske vægt af reagenser udstedt af producenterne mindre end 10% (eller langt mindre end denne værdi) af beholderen. Det meste af vægten kommer fra tøris, ispakker og skumkasser, så transportomkostningerne er ekstremt høje.
I marts 2020 begyndte Covid-19 at bryde ud i en stor skala i udlandet, og efterspørgslen efter nye coronavirus nukleinsyretektionsreagens steg dramatisk. På trods af de høje omkostninger ved eksport af reagenserne i den kolde kæde, kan de fleste producenter stadig acceptere den på grund af den store mængde og høje fortjeneste.
Men med forbedring af nationale eksportpolitikker for anti-pandemiske produkter såvel som opgradering af national kontrol over strømmen af mennesker og logistik, er der udvidelse og usikkerhed i reagensernes transporttid, hvilket resulterede i fremtrædende produktproblemer forårsaget ved transporten. Udvidet transporttid (transporttid på cirka en halv måned er meget almindelig) fører til hyppige produktfejl, når produktet når klienten. Dette har urolig de fleste nukleinsyre -reagenser eksportvirksomheder.
Lyophiliseret teknologi til PCR -reagens hjalp transporten af nye coronavirus nukleinsyretektionsreagens over hele verden
De lyofiliserede PCR -reagenser kan transporteres og opbevares ved stuetemperatur, hvilket ikke kun kan reducere transportomkostningerne, men også undgå kvalitetsproblemerne forårsaget af transportprocessen. Derfor er lyofilisering af reagenset den bedste måde at løse problemet med eksporttransport på.
Lyofilisering involverer at fryse en opløsning i en fast tilstand og derefter sublimere og adskille vanddampen under vakuumtilstand. Det tørrede opløste stof forbliver i beholderen med den samme sammensætning og aktivitet. Sammenlignet med konventionelle flydende reagenser har den fuldkomponent lyofiliserede nye coronavirus nukleinsyre-detektionsreagens produceret ved at LIMING BIO følgende egenskaber:
Ekstremt stærk varmestabilitet: Det kan med standbehandling ved 56 ℃ i 60 dage, og reagensens morfologi og ydeevne forbliver uændret.
Normal temperaturopbevaring og transport: Intet behov for koldkæde, ikke nødvendigt at opbevare ved lav temperatur, før du ikke forsegle, frigør koldopbevaringspladsen fuldt ud.
Klar til brug: Lyofilisering af alle komponenter, ikke behov for systemkonfiguration, undgå tab af komponenter med høj viskositet såsom enzym.
Multiplex -mål i et rør: Detektionsmålet dækker nyt coronavirus orf1ab -gen, N -gen, S -gen for at undgå virusgenovariation. For at reducere falsk negativ bruges human RNase P -genet som intern kontrol for at imødekomme det kliniske behov for prøvekvalitetskontrol.
SARS-COV-2 IgM/IgG Antistof Rapid Test og Novel Coronavirus (SARS-CoV-2) Multiplex Real-Time PCR-kit (detektion for tre gener) er tidligere blevet markeret i Storbritannien og nu accepteret og behandlet af EUA af FDA i Amerika.
Nanjing Liming Bio-Products Co., Ltd. har altid sat kvaliteten af testkittet i første omgang og koncentrerer sig om udvidelsen af kapaciteten. Virksomheden leverer test af produkter og tjenester af høj kvalitet til medicinske institutioner over hele verden og bidrager til den globale epidemiske forebyggelse og -kontrol for at opbygge et globalt samfund af delt fremtid.
Lang presse ~ scan og følg os
E -mail:sales@limingbio.com
Hjemmeside: https://limingbio.com

Posttid: Jul-06-2020







